

























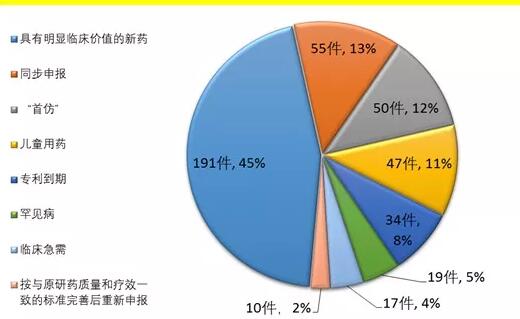
日前,CDE官网发布2017年度药品审评报告,从文中得知,截至2017年底,药审中心共将25批423件注册申请纳入优先审评程序,其中具有明显临床价值的新药占比最大,共191件,占45%,儿童用药共47件。纳入优先审评程序的注册申请情况详见下图。
截至2017年底,纳入优先审评程序的423件注册申请中已有272件完成审评,占比为64%。自纳入优先审评程序之日起,IND申请、NDA、ANDA首轮审评平均用时分别为39个工作日、59个工作日和81个工作日。
截至2017年底,共有110件注册申请通过优先审评程序得以加快批准上市(以通用名计算,共涉及57个品种),其中,2017年有50个品种,具体品种名单详下表。包括国产自主研发的创新药重组埃博拉病毒病疫苗、口服丙肝治疗用新药阿舒瑞韦软胶囊、非小细胞肺癌靶向药甲磺酸奥希替尼片、儿童抗癫痫用药左乙拉西坦注射用浓溶液、治疗乙肝和艾滋病的国产仿制药富马酸替诺福韦二吡呋酯胶囊等一批具有明显临床价值的药品通过优先审评程序得以加快、优先批准上市,为满足临床用药需求、降低用药费用、促进公众健康提供了有效保障。
序号 | 药品名称 | 纳入优先审评的理由 |
1 | 阿柏西普眼内注射溶液 | 具有明显临床价值的新药 |
2 | 阿达木单抗注射液 | 具有明显临床价值的新药 |
3 | 阿法替尼片 | 具有明显临床价值的新药 |
4 | 阿舒瑞韦软胶囊 | 具有明显临床价值的新药 |
5 | 艾曲泊帕片 | 具有明显临床价值的新药 |
6 | 奥比帕利片 | 具有明显临床价值的新药 |
7 | 达比加群酯胶囊 | 具有明显临床价值的新药 |
8 | 达塞布韦片 | 具有明显临床价值的新药 |
9 | 德谷胰岛素注射液 | 具有明显临床价值的新药 |
10 | 地塞米松玻璃体内植入剂 | 具有明显临床价值的新药 |
11 | 多替阿巴拉米片 | 具有明显临床价值的新药 |
12 | 枸橼酸托法替布片 | 具有明显临床价值的新药 |
13 | 甲苯磺酸索拉非尼片 | 具有明显临床价值的新药 |
14 | 甲磺酸奥希替尼片 | 具有明显临床价值的新药 |
15 | 甲磺酸雷沙吉兰片 | 具有明显临床价值的新药 |
16 | 利奥西呱片 | 具有明显临床价值的新药 |
17 | 利伐沙班片 | 具有明显临床价值的新药 |
18 | 磷酸芦可替尼片 | 具有明显临床价值的新药 |
19 | 马昔腾坦片 | 具有明显临床价值的新药 |
20 | 氢溴酸伏硫西汀片 | 具有明显临床价值的新药 |
21 | 瑞戈非尼片 | 具有明显临床价值的新药 |
22 | 沙库巴曲缬沙坦钠片 | 具有明显临床价值的新药 |
23 | 舒更葡糖钠注射液 | 具有明显临床价值的新药 |
24 | 索磷布韦片 | 具有明显临床价值的新药 |
25 | 维莫非尼片 | 具有明显临床价值的新药 |
26 | 西美瑞韦胶囊 | 具有明显临床价值的新药 |
27 | 盐酸达拉他韦片 | 具有明显临床价值的新药 |
28 | 伊布替尼胶囊 | 具有明显临床价值的新药 |
29 | 乙磺酸尼达尼布软胶囊 | 具有明显临床价值的新药 |
30 | 茚达特罗格隆溴铵吸入粉雾剂用胶囊 | 具有明显临床价值的新药 |
31 | 重组埃博拉病毒病疫苗 | 具有明显临床价值的新药 |
32 | 注射用阿扎胞苷 | 具有明显临床价值的新药 |
33 | 注射用艾普拉唑钠 | 具有明显临床价值的新药 |
34 | 富马酸替诺福韦二吡呋酯片 | 临床急需 |
35 | 来那度胺胶囊 | 临床急需 |
36 | 左乙拉西坦注射用浓溶液 | 儿童用药 |
37 | 醋酸加尼瑞克注射液 | 首仿 |
38 | 丁酸氯倍他松乳膏 | 首仿 |
39 | 富马酸替诺福韦二吡呋酯胶囊 | 首仿 |
40 | 酒石酸利斯的明胶囊 | 首仿 |
41 | 拉坦噻吗滴眼液 | 首仿 |
42 | 洛索洛芬钠凝胶膏 | 首仿 |
43 | 曲伏前列素滴眼液 | 首仿 |
44 | 吸入用乙酰半胱氨酸溶液 | 首仿 |
45 | 苯磺顺阿曲库铵注射液 | 同步申报 |
46 | 缬沙坦片 | 同步申报 |
47 | 注射用阿奇霉素 | 同步申报 |
48 | 注射用培美曲塞二钠 | 同步申报 |
49 | 注射用帕瑞昔布钠 | 专利到期 |
50 | 注射用硼替佐米 | 专利到期 |
2017年,一批具有明显临床价值的创新药、临床急需药、专利到期药和我国首仿药通过技术审评建议批准上市。
抗肿瘤药物
1.甲磺酸奥希替尼片:为全球首个第三代晚期肺癌靶向药,适用于既往经表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)治疗时或治疗后出现疾病进展,并且经检测确认存在EGFR T790M突变阳性的局部晚期或转移性非小细胞性肺癌(NSCLC)
成人患者的治疗。肺癌是我国发病率和死亡率最高的恶性肿瘤,对于上述患者目前尚无有效的治疗药物,存在明确的临床急需。该药品针对上述患者具有较好的治疗效果,安全性可以耐受,为上述特定的患者人群提供了新的治疗选择。
2.伊布替尼胶囊:为Bruton酪氨酸激酶(BTK)抑制剂,适用于治疗既往至少接受过一种治疗的套细胞淋巴瘤和慢性淋巴细胞白血病患者。该药品是全球首个全新作用机制的治疗慢性淋巴细胞白血病药物,为慢性淋巴细胞白血病患者带来更多的治疗选择。
3.维莫非尼片:为一种小分子BRAF丝氨酸-苏氨酸激酶抑制剂,适用于治疗BRAF V600突变阳性的不能切除或转移性黑色素瘤。该药品是全球首个治疗恶性黑色素瘤的靶向药物,可有效提高患者用药的可及性。
4.磷酸芦可替尼片:为小分子JAK1/JAK2激酶(Janus相关激酶)抑制剂,适用于治疗中危或高危的骨髓纤维化。骨髓纤维化是罕见的骨髓增殖性肿瘤疾病,目前国内尚无明确有效治疗手段,该药品为全球首个用于治疗骨髓纤维化药物,可有效提高患者用药的可及性。
抗感染药物
5.盐酸达拉他韦片、6.阿舒瑞韦软胶囊、7.西美瑞韦胶囊、8.索磷布韦片、9.奥比帕利片、10.达塞布韦片:为直接抗丙型肝炎病毒(HCV)药物,适用于治疗成人慢性丙型肝炎(CHC)。我国约有1000万丙型肝炎患者,上述药物批准上市有效解决了我国没有直接抗病毒药物的局面,为我国慢性丙肝患者提供了有效的突破性治疗手段。
11.多替阿巴拉米片:为含有多替拉韦、阿巴卡韦和拉米夫定3种成分的新型抗人类免疫缺陷病毒(HIV)感染的固定剂量复方制剂,适用于治疗成人和12岁及以上的青少年的HIV感染。目前治疗艾滋病药物有不良反应发生率高、耐受性差、药物相互作用多等缺点,且长期服药存在耐药可能,该药品较已上市的治疗方案有一定的临床优势,为临床增加新的治疗选择。
风湿性疾病及免疫药物
12.枸橼酸托法替布片:为Janus激酶(包括JAK3)选择性抑制剂,适用于治疗对甲氨蝶呤疗效不足或对其无法耐受的中度至重度活动性类风湿关节炎(RA)成年患者,可作为单药治疗,或者与甲氨蝶呤或其他非生物改善病情抗风湿药(DMARD)联合使用。该药品是全球首个口服治疗类风湿关节炎的靶向药物,将为风湿关节炎患者带来更多的治疗选择。
内分泌系统药物
13.达格列净片:为高选择性的人体肾脏钠葡萄糖共转运体(SGLT2)抑制剂,适用于II型糖尿病患者单药治疗。该药品是全球首个全新作用机制的口服降糖药物,可有效提高患者用药的可及性。
循环系统药物
14.沙库巴曲缬沙坦钠片:为血管紧张素受体脑啡肽酶抑制剂,适用于治疗伴有射血分数降低的慢性心脏衰竭患者(心功能Ⅱ-Ⅳ级),以降低心血管死亡和心力衰竭住院的风险。该药品是近二十年来全球慢性心衰治疗领域的突破性创新药物,在减少心血管死亡、全因死亡、心衰住院(包括首次住院和全部住院),以及改善症状和患者报告结局方面,超过目前指南推荐的循证治疗,可为临床增加新的治疗选择。
皮肤五官药物
15.康柏西普眼用注射液:为国内首个适用于治疗继发于病理性近视的脉络膜新生血管引起的视力损伤的生物制品药物。由于城市化进程加快,用眼过度现象普遍存在,病理性近视引起的视力损伤并导致失明的发病人数呈上升趋势,该药品批准上市对有效提高此类病症患者的临床用药可及性具有积极意义。
16.阿达木单抗注射液:为重组人免疫球蛋白(IgG1)单克隆抗体,新增适应症适用于需要进行系统治疗或光疗、并且对其他系统治疗(包括环孢素、甲氨蝶呤或光化学疗法)不敏感、或具有禁忌症、或不能耐受的成年中重度慢性斑块状银屑病患者。该药品为国内首个全人源的TNFα单抗,在抗药抗体产生及安全性方面具有一定优势,为临床带来一种更安全且有效的治疗选择。
神经系统药物
17.甲磺酸雷沙吉兰片:为选择性不可逆单胺氧化酶-B(MAO-B)抑制剂,适用于治疗原发性帕金森病。该药品在国外用于帕金森病早期的一线单药治疗,或与左旋多巴联用治疗中、重度帕金森病,可有效提高患者用药的可及性。
消化系统药物
18.艾普拉唑肠溶片:为首个国产质子泵抑制剂创新药,新增适应症适用于治疗反流性食管炎,为临床提供更多有效治疗选择,增加了临床可及性。
呼吸系统药物
19.丹龙口服液:为新的中药复方制剂,适用于治疗中医热哮证、支气管哮喘患者。该药品为我国上市许可持有人制度试点实施以来首个获批的中药新药品种,为哮喘病患者提供一种全新的安全有效的治疗方案,对提高患者的生存质量具有重要意义。
预防用生物制品(疫苗)
20.重组埃博拉病毒病疫苗(腺病毒载体):为我国自主研发的重组埃博拉疫苗,也是全球首个2014基因突变型埃博拉疫苗。药审中心按照有条件批准程序完成了该疫苗上市申请的审评,该药品对于应对埃博拉疫情的公共卫生需求和完成国家战略储备具有重大意义。

